
- Avtor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:40.
- Nazadnje spremenjeno 2025-01-22 17:09.
X = [Fe(SCN)2+] in je treba določiti iz standardne krivulje. Nato lahko izračunate ravnotežna konstanta , Keq , uporabljati ravnotežje koncentracije. Standardna krivulja je graf Absorbanca v primerjavi z [Fe(SCN)2+] (slika 8.1). Uporabimo ga lahko, da dobimo koncentracijo raztopine, ko dobimo absorbance.
Ob upoštevanju tega, kako najdete ravnotežno koncentracijo iz absorbance?
Zato [Fe(SCN)2+]ekv je mogoče določiti neposredno iz absorbance meritve. Ravnotežne koncentracije reaktantov lahko izračunamo tako, da odštejemo ravnotežna koncentracija izdelka od začetne koncentracije reaktantov.
Drugič, kaj je FeSCN? The FeSCN 2+ kompleks, ki nastane kot posledica reakcije med železovimi (III) in tiocianatnimi ioni, ima zelo intenzivno krvno rdečo barvo (ali oranžno v razredčeni raztopini), kar omogoča enostavno odkrivanje in kvantitativno določanje s spektrofotometrijo. Reaktanti (Fe3+ in SCN-) sta praktično brezbarvna.
Kako na ta način najdete ravnotežno koncentracijo iz Beerovega zakona?
ravnotežna koncentracija produkta
- [FeSCN2+] v ravnovesju se določi z uporabo Beerovega zakona; x je količina FeSCN2+ ustvarjeno (določeno eksperimentalno).
- x = [FeSCN 2+] ekv =
- a.
- Uporabite Eq.
- Poiščite povprečno vrednost Kekv, standardni odklon in relativna napaka (standardna deviacija, deljena s povprečjem).
Kaj pomeni KEQ?
Keq samo pove, kaj bo v ravnotežju prednostno. Od Keq = [izdelki]/[reaktanti] velika vrednost k (k>>1) pomeni, da bo reakcija produktom veliko bolj dajala prednost, kar pomeni, da boste imeli večinoma produkte, ko bo reakcija dosegla ravnotežje.
Priporočena:
Kako izračunate ravnotežno silo?

Neto sila mora biti nič Neto sila, ki deluje na predmet, mora biti nič. Zato se vse sile uravnotežijo v vsaki smeri. Na primer, avtomobil, ki se giblje po avtocesti s konstantno hitrostjo, je v ravnotežju, saj ne pospešuje v nobeni smeri naprej ali navpično. Matematično je to navedeno kot Fnet = ma = 0
Kako najdete konstanto sorazmernosti v grafu?
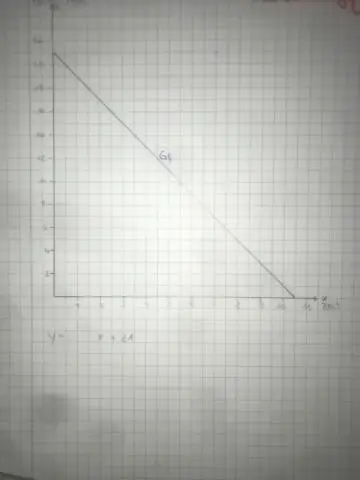
Če želite poiskati svojo konstanto sorazmernosti iz grafa, sledite tem korakom: Poiščite dve enostavni točki. Začnite z skrajno levo točko in preštejte, koliko kvadratov morate dvigniti, da pridete do druge točke. Preštejte, koliko kvadratov morate iti na desno. Poenostavite in našli boste svojo konstanto sorazmernosti
Ali dolžina vzmeti vpliva na konstanto vzmeti?

Na splošno je vzmetna konstanta vzmeti obratno sorazmerna z dolžino vzmeti, ob predpostavki, da govorimo o vzmeti določenega materiala in debeline
Kakšna je razlika med kontrolo in konstanto v znanosti?

Razlike med konstanto in kontrolo Konstantna spremenljivka se ne spremeni. Po drugi strani se kontrolna spremenljivka spreminja, vendar se namerno ohranja konstantna skozi ves poskus, da pokaže razmerje med odvisnimi in neodvisnimi spremenljivkami
Kako je razpolovna doba reakcije ničelnega reda povezana z njeno konstanto hitrosti?

V kinetiki ničelnega reda hitrost reakcije ni odvisna od koncentracije substrata. Formula t 1 /2 za reakcijo ničelnega reda kaže, da je razpolovna doba odvisna od količine začetne koncentracije in hitrostne konstante
