
- Avtor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:40.
- Nazadnje spremenjeno 2025-06-01 05:06.
Sinteza in reaktivnost
Po prvem poskusu sinteze leta 1903 je pripravil Otto Ruff dušikov trifluorid z elektrolizo staljene zmesi amonijevega fluorida in vodikovega fluorida.
Poleg tega, kako se proizvaja dušikov trifluorid?
Proizvodnja NF3 z elektrolizo v staljenih fluoridih npr. dušikov trifluorid (NF3) je stabilen plin pri sobni temperaturi in ima močno oksidacijsko moč pri višjih temperaturah [3-5]. Do 200 °C je njegova reaktivnost primerljiva s kisikom. Nad 400 °C je reaktivnost NF3 postane bolj podoben fluoru.
Lahko se tudi vprašamo, kakšna vrsta vezi je dušikov trifluorid? Molekula ima trigonalno piramidno strukturo, kot je amoniak. The vez kot se zmanjša s 107° v amoniaku na 101,9° v NF3, ker zelo elektronegativni fluori potegnejo elektrone v N-F obveznice proti sebi, zmanjševanje medelektronskih odbojov, tako da NF3 'dežnik' se zapre.
Poleg tega, kakšna je kemična formula za dušikov trifluorid?
NF3
Ali je nf3 oksidant?
dušikov trifluorid ( NF3 ) je zanimiv kot oksidant visokoenergijskih goriv, za pripravo tetrafluorohidrazina in za fluoriranje fluoroogljikovih olefinov. Brezbarven, negorljiv, utekočinjen plin z zaznavnim vonjem. zelo strupeno; Draži zračne poti. Močna oksidant.
Priporočena:
Kako nastane medialna morena?
Medialna morena je greben morene, ki poteka po središču dna doline. Nastane, ko se srečata dva ledenika in se naplavin na robovih sosednjih stranic doline združijo in odnesejo na vrh povečanega ledenika
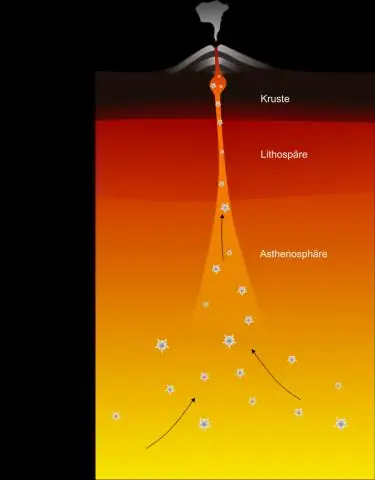
Kako nastane vroča točka?

Vulkanska 'vroča točka' je območje v plašču, iz katerega se toplota dviga kot toplotni oblak iz globine Zemlje. Visoka toplota in nižji tlak na dnu litosfere (tektonske plošče) olajšata taljenje kamnine. Ta talina, imenovana magma, se dviga skozi razpoke in izbruhne, da tvori vulkane
Kako nastane molekula vode?

Molekula vode nastane, ko se dva atoma vodika kovalentno povežeta z atomom kisika. V kovalentni vezi so elektroni razdeljeni med atome. Atom kisika močneje privlači elektrone kot vodik. To daje vodi asimetrično porazdelitev naboja
Kako se imenuje sol, ki nastane z nevtralizacijo klorovodikove kisline in natrijevega hidroksida?
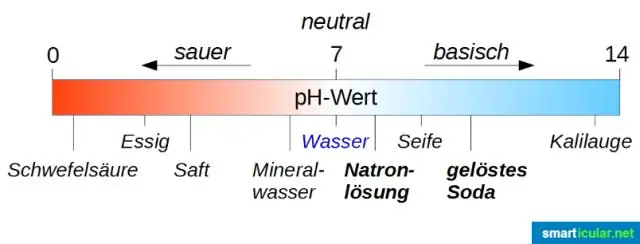
Pojasnilo: Reakcija med natrijevim hidroksidom (NaOH) in klorovodikovo kislino (HCl) je nevtralizacijski proces, ki povzroči tvorbo soli, natrijevega klorida (NaCl) in vode (H2O). To je eksotermna reakcija
Kakšen je postopek, s katerim se nitratni ioni in nitritni ioni pretvorijo v plin dušikov oksid in dušikov plin n2?

Nitratni ioni in nitritni ioni se pretvorijo v plin dušikov oksid in dušikov plin (N2). Korenine rastlin absorbirajo amonijeve ione in nitratne ione za uporabo pri izdelavi molekul, kot so DNK, aminokisline in beljakovine. Organski dušik (dušik v DNK, aminokislinah, beljakovinah) se razgradi na amoniak, nato amoniak
