
- Avtor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:40.
- Nazadnje spremenjeno 2025-01-22 17:09.
Reševanje problema kislinsko-bazične nevtralizacije
- Korak 1: Izračunaj število molov OH-. Molarnost = moli/ glasnost . mol = molarnost x Glasnost . moli OH- = 0,02 M/100 mililitrov.
- 2. korak: Izračunajte prostornino HCl potrebno . Molarnost = moli/ glasnost . Glasnost = mol/molarnost. Glasnost = moli H+/0,075 Molarnost.
Podobno se sprašuje, kako nevtralizirati močno bazo?
Uporabite šibko kislino za nevtralizirati baze . Primeri vključujejo natrijev hidroksid, kalijev hidroksid in amoniak. Veliko različnih izdelkov pomaga pri nevtralizacija kislin in podlage . Lahko so tako preprosti kot vrečka citronske kisline ali natrijevega seskvikarbonata ali pa tako zapleteni kot strjevalnik in nevtralizator skupaj.
Poleg tega, ali je za nevtralizacijo močne kisline potrebno več baze? Močne kisline volja nevtralizirajo močne baze enakih koncentracij v enakih količinah. Več glasnost šibkega kislina je potrebno za nevtralizirajo močno bazo če so koncentracije enake in obratno za šibke podlage in močne kisline . Pufer je raztopina, ki vsebuje šibko kislina in sol z istim anionom kot kislina.
Od tega, koliko molov NaOH je potrebnih za nevtralizacijo kisline?
1 odgovor. Potrebujete 3 mol natrijevega hidroksida do nevtralizirati 1 mol fosforja kislina.
Ko naredimo kislo raztopino bazično Kako to storiti?
Dodajanje kislina poveča koncentracijo H3O+ ioni v rešitev . Dodajanje a bazo zmanjša koncentracijo H3O+ ioni v rešitev . An kislina in a osnova so kot kemična nasprotja. Če bazo je dodan v an kisla raztopina , rešitev postane manj kislo in se premika proti sredini pH lestvici.
Priporočena:
Kako se imenuje sol, ki nastane z nevtralizacijo klorovodikove kisline in natrijevega hidroksida?
Pojasnilo: Reakcija med natrijevim hidroksidom (NaOH) in klorovodikovo kislino (HCl) je nevtralizacijski proces, ki povzroči tvorbo soli, natrijevega klorida (NaCl) in vode (H2O). To je eksotermna reakcija
Kaj bi se zgodilo, če bi pufrirani raztopini dodali majhno količino kisline?

Nastane z mešanjem velike količine šibke kisline ali šibke baze z njeno konjugirano bazo ali kislino. Ko ji dodate majhne količine kisline ali alkalije (baze), se njen pH ne spremeni bistveno. Z drugimi besedami, puferska raztopina prepreči, da bi se kislina in baza nevtralizirala
Koliko kisline je potrebno za nevtralizacijo baze?

Titracije. Ko klorovodikova kislina reagira z natrijevim hidroksidom, je za popolno nevtralizacijo potrebno molsko razmerje kislina/baza 1:1. Če bi namesto tega klorovodikova kislina reagirala z barijevim hidroksidom, bi bilo molsko razmerje 2:1. Za popolno nevtralizacijo enega mola Ba(OH)2 sta potrebna dva mola HCl
Kako uporabljamo kisline in baze v vsakdanjem življenju?

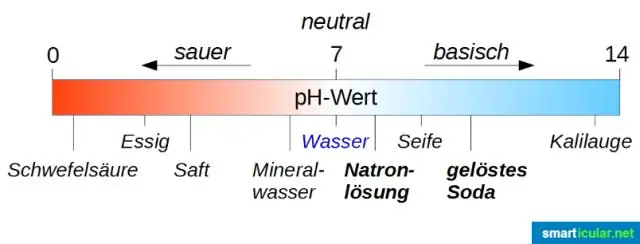
Zobna pasta in antacidi so dobri primeri osnovnih izdelkov, medtem ko so živila, kot sta pomarančni sok ali pomaranče, zelo kisla. PH lestvica. Lestvica pH sega od 1 do 14 in prikazuje obseg kislin in baz od zgoraj navzdol. Zobna pasta in pH. pH živilskih izdelkov. Zdravila za nevtralizacijo kisline. Čistilni izdelki
Zakaj je za nevtralizacijo šibke kisline potrebno več baze?

Šibka kislina disociira na H+ in njeno konjugirano bazo, ki ustvari pufer. Ta se upira spremembam pH in zahteva več baze, da jo nevtralizira. Dodajanje šibke kisline vodi samo po sebi ne ustvari pufra. Zato se lahko zdi, da šibka kislina potrebuje več baze, ker je dvig pH veliko počasnejši
